| Wirus BK | |
|---|---|
 |
|
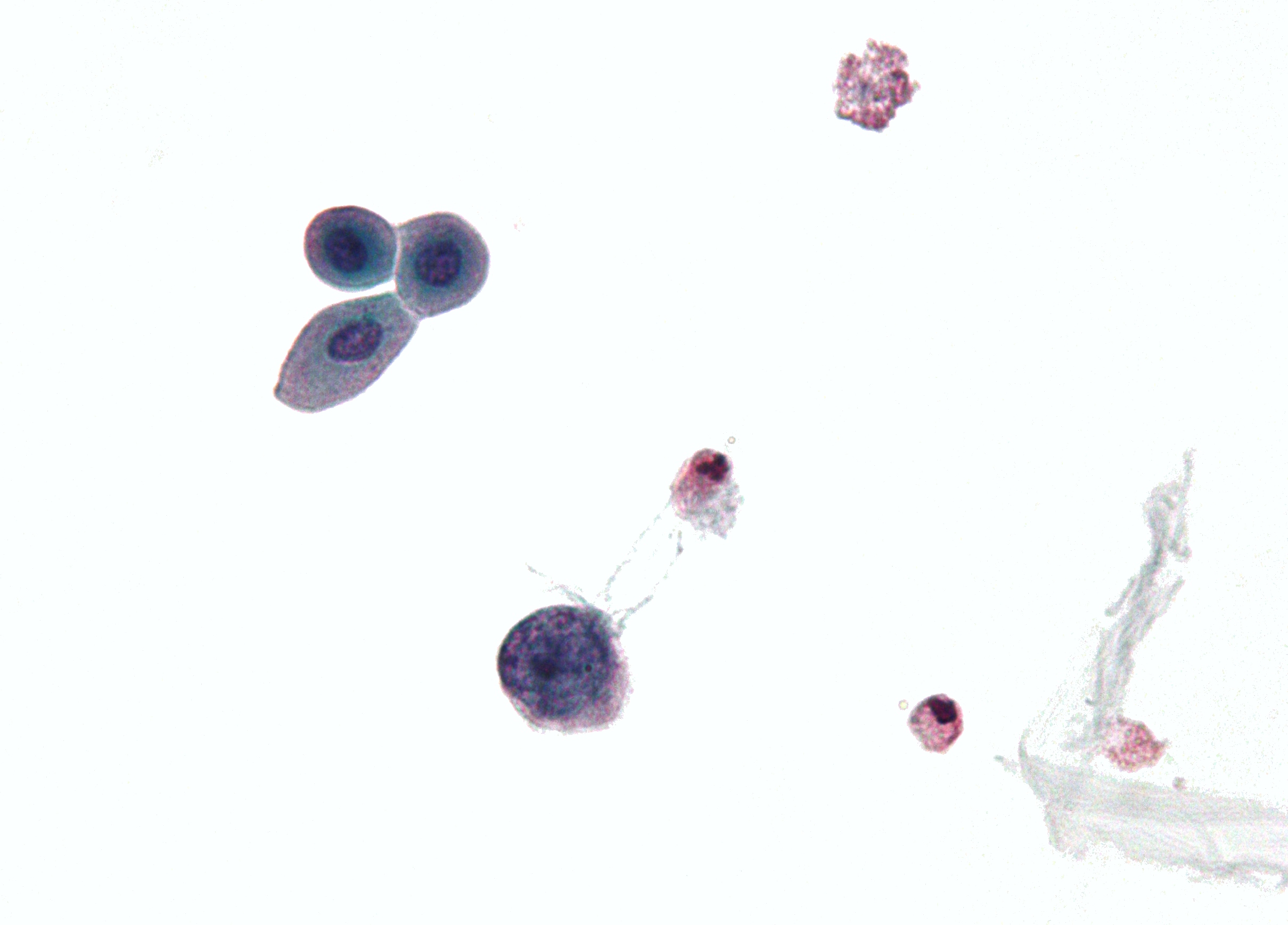
| Mikrofotografia przedstawiająca komórkę zakażoną poliomawirusem – dużą (niebieską) komórkę poniżej środkowej lewej strony. Materiał cytologiczny moczu. | |
| Specjalność | Choroba zakaźna |
Plik Wirus BK jest członkiem rodziny poliomawirusów. Zakażenie wirusem BK jest powszechne, ale istotne konsekwencje zakażenia są rzadkie, z wyjątkiem osób z obniżoną odpornością i osób z obniżoną odpornością. Wirus BK to skrót imienia pierwszego pacjenta, od którego wirus został wyizolowany w 1971 roku (pacjent miał wtedy 29 lat).
Objawy zakażenia wirusem BK
Wirus BK rzadko powoduje chorobę, ale zazwyczaj jest związany z pacjentami, którzy przeszli przeszczep nerki; wiele osób zarażonych tym wirusem przebiega bezobjawowo. Jeśli objawy się pojawią, są zwykle łagodne: infekcja dróg oddechowych lub gorączka. Są to objawy pierwotnych zakażeń BK. Chociaż bez objawów klinicznych, ślady wirusa BK wykryto w próbkach kobiet dotkniętych samoistnym poronieniem. Przeciwciała w surowicy przeciw wirusowi BK wykryto również u kobiet po poronieniu samoistnym, a także u kobiet, które dobrowolnie przerwały ciążę.
Wirus przenosi się następnie do nerek i dróg moczowych, gdzie utrzymuje się przez całe życie jednostki. Uważa się, że nawet 80% populacji zawiera utajoną postać tego wirusa, która pozostaje utajona, dopóki organizm nie przejdzie jakiejś formy immunosupresji. Zwykle ma to miejsce w przypadku przeszczepu nerki lub przeszczepu wielu narządów. Prezentacja u tych osób z obniżoną odpornością jest znacznie poważniejsza. Objawy kliniczne obejmują dysfunkcję nerek (objawiającą się postępującym wzrostem stężenia kreatyniny w surowicy) oraz nieprawidłową analizę moczu ujawniającą komórki kanalików nerkowych i komórki zapalne.
Przyczyna
Przenoszenie wirusa
Lekarze nie wiedzą, w jaki sposób przenosi się ten wirus. Ale lekarze wiedzą, że wirus przenosi się z człowieka na człowieka, a nie ze źródła zwierzęcego. Sugerowano, że wirus ten może być przenoszony przez drogi oddechowe lub mocz, ponieważ osoby zakażone okresowo wydalają wirusa z moczem. Badanie przeprowadzone na 400 zdrowych dawcach krwi wykazało, że 82% było pozytywnych na obecność IgG przeciwko wirusowi BK.
Czynniki ryzyka
U niektórych pacjentów po przeszczepieniu nerki konieczne zastosowanie leków immunosupresyjnych powoduje efekt uboczny polegający na umożliwieniu replikacji wirusa w przeszczepie, chorobie zwanej nefropatią BK.
U 1–10% pacjentów po przeszczepieniu nerki następuje progresja do nefropatii związanej z wirusem BK (BKVAN), a do 80% tych pacjentów traci przeszczep. Początek zapalenia nerek może wystąpić już od kilku dni po przeszczepie do nawet 5 lat.
Jest to również związane ze zwężeniem moczowodu i śródmiąższowym zapaleniem nerek. U biorców przeszczepu szpiku kostnego jest to zauważalne jako przyczyna krwotocznego zapalenia pęcherza.
Miano wiremii BK> 185 000 kopii / ml w czasie pierwszej pozytywnej diagnozy BKV – aby być najsilniejszym predyktorem BKVAN (97% swoistość i 75% czułość). Ponadto stwierdzono, że szczytowe miano wirusa BKV we krwi, osiągające 223 000 kopii / ml w dowolnym czasie, jest czynnikiem predykcyjnym dla BKVAN (swoistość 91% i czułość 88%).
Diagnoza zakażenia wirusem BK
Wirus ten można zdiagnozować za pomocą badania krwi BKV lub testu moczu na komórki wabika, oprócz wykonania biopsji nerek. W celu identyfikacji wirusa często przeprowadza się techniki PCR.
Leczenie infekcji wirusem BK
Podstawą terapii jest zmniejszenie immunosupresji. Niedawny wzrost BKVAN koreluje ze stosowaniem silnych leków immunosupresyjnych, takich jak takrolimus i mykofenolan mofetylu (MMF). Badania nie wykazały żadnej korelacji między BKVAN a pojedynczym lekiem immunosupresyjnym, ale raczej ogólne obciążenie immunosupresyjne.
- Nie ma wytycznych ani poziomów i dawek leków, które umożliwiałyby właściwą redukcję immunosupresantów w BKVAN
- Najpopularniejsze metody:
- Wycofanie MMF lub takrolimusu
- Zastąpienie takrolimusu cyklosporyną
- Ogólne zmniejszenie obciążenia immunosupresyjnego
- Zgłaszano, że niektóre minimalne stężenia cyklosporyny spadły do 100–150 ng / ml, a poziomy takrolimusu do 3–5 ng / ml
- Retrospektywna analiza 67 pacjentów wykazała, że przeżycie przeszczepu było podobne między redukcją a odstawieniem leków.
- Badanie jednoośrodkowe wykazało, że alloprzeszczepy nerki zostały zachowane u 8/8 osób, u których zastosowano zmniejszenie immunosupresji, podczas gdy utrata przeszczepu wystąpiła u 8/12 pacjentów leczonych zwiększoną terapią z powodu odrzucenia narządu.
Inne opcje terapeutyczne obejmują Leflunomid, Cidofovir, IVIG i fluorochinolony. Leflunomid, inhibitor syntezy pirymidyny, jest obecnie ogólnie akceptowany jako druga opcja leczenia po zmniejszeniu immunosupresji.
Leflunomid w BKVAN
Uzasadnienie stosowania leflunomidu w BKVAN wynika z jego połączonych właściwości immunosupresyjnych i przeciwwirusowych. W dwóch badaniach obejmujących 26 i 17 pacjentów, u których rozwinęło się BKVAN w trzylekowym schemacie z takrolimusem, MMF i steroidami, zastąpiono MMF leflunomidem w dawce 20–60 mg na dobę. 84% i 88% pacjentów miało odpowiednio klirens lub stopniowe zmniejszenie miana wirusa oraz stabilizację lub poprawę funkcji przeszczepu. W badaniu Teschner i wsp. w 2009 roku 12/13 pacjentów, u których wymieniono MMF na leflunomid, usunęło wirusa do 109 dni. W serii przypadków stwierdzono poprawę lub stabilizację u 23/26 pacjentów z BKVAN po zmianie MMF na leflunomid.
Nie ma wytycznych dotyczących dawkowania leflunomidu w BKVAN. Różnice między pacjentami i pacjentami sprawiły, że dawkowanie i monitorowanie leflunomidu były niezwykle trudne.
- Badanie z udziałem 26 i 17 pacjentów otrzymywało dawki od 20 mg / dobę do 60 mg / dobę z minimalnym stężeniem 50-100 µg / ml. Niepowodzenie obserwowano u pacjentów ze stężeniem leflunomidu w osoczu <40 µg / ml.
- W jednym badaniu z udziałem 21 pacjentów stwierdzono, że niskie poziomy (<40 µg / ml) i wysokie (> 40 µg / ml) miały podobny wpływ na szybkość usuwania wirusa. Osoby z wyższymi poziomami miały więcej zdarzeń niepożądanych (hematologiczne, wątrobowe).
- W badaniu Teschner i wsp. Dawki i stężenie leku nie wykazały korelacji z istotnymi różnicami w zależności od osoby.
- W badaniu Teschnera niskie stężenia leku były związane ze zmniejszeniem miana wirusa. Utrudnia to ustalenie, czy przyczyną klirensu wirusa było zmniejszenie wiremii lub dodanie leflunomidu.
Inne opcje leczenia
- Antybiotyki chinolonowe: wykazano, że cyprofloksacyna (Cipro) znacznie obniża miano wirusa, ale nie ma danych dotyczących przeżycia i utraty przeszczepu.
- Immunoglobulina dożylna (IVIG) ma zastosowanie w leczeniu infekcji i odrzuceniu przeszczepu allogenicznego – trudne do rozróżnienia
- Cidofovir ma ograniczone dane i jest silnie nefrotoksyczny.
Historia
Wirus BK został po raz pierwszy wyizolowany w 1971 r. Z moczu pacjenta po przeszczepie nerki, inicjały BK Wirus BK jest podobny do innego wirusa zwanego wirusem JC (JCV), ponieważ ich genomy mają 75% podobieństwa sekwencji. Oba te wirusy można zidentyfikować i odróżnić od siebie, przeprowadzając testy serologiczne z użyciem specyficznych przeciwciał lub stosując metodę genotypowania opartą na PCR.
.













:max_bytes(150000):strip_icc()/GettyImages-99291331-58ab566f3df78c345b0c137c.jpg)
:max_bytes(150000):strip_icc()/tb-skin-test-5176447-Final-8edd99bb6eef47c989e3e351ea793282.jpg)

Discussion about this post